B 塩化ナトリウム水溶液に硝酸銀水溶液を加えると,白色の沈殿が生じる。 c 大理石に希塩酸を注いだときに発生する気体を石灰水に通じると,白くにごる。 ① aのみ ② bのみ ③ cのみ ④ aとb ⑤ aとc ⑥ bとc沈殿 化学変化 化学反応式 石灰水(水炭酸カルシウム)+二酸化炭素 →炭酸カルシウム(白色沈殿)+水 Ca(OH)2+CO2→CaCO3+H2O 塩化ナトリウム+硝酸銀 →塩化銀(白色沈殿)+硝酸ナトリウム硝酸銀水溶液にアンモニア水を加えると、一時的に少量の水酸化銀 AgOH の白色沈殿ができる。Ag OH – → AgOH ↓ この水酸化銀 AgOH は不安定で、すぐに酸化銀 Ag 2 O の暗褐色沈殿となる。 2Ag 2OH – → Ag 2 O ↓ H 2 O
質問箱
硝酸銀 白色沈殿 化学式
硝酸銀 白色沈殿 化学式-銀イオンに塩化物イオンを加えると,塩化銀AgClの白色沈殿ができることを知っていますね。 8-9 銅と銀の酸化力のある酸との化学反応式 銀と濃硝酸 ag 2hno 3 → agno 3 no 2 h 2 o 銀と希硝酸 3ag 4hno 3 → 3agno 3 no 2h 2 o 銀と熱濃硫酸 2ag 2h 2 so 4 → ag 21/121 覚えたい元素記号と化学式 何度も繰り返して覚えよう! 元素記号 は原子番号を示す。 44!これだけ覚えれば,大学入試も完璧です。 1水素 H 2ヘリウム He 3リチウム Li 4ベリリウム Be 5ホウ素 B 6炭素 C 7窒素(チッ素) N 8酸素 O 9フッ素 F



化学基礎112c 化学基礎05 13硝酸銀水溶液白色沈殿塩化銀塩素塩化物イオン炎色反応ナトリウム Youtube
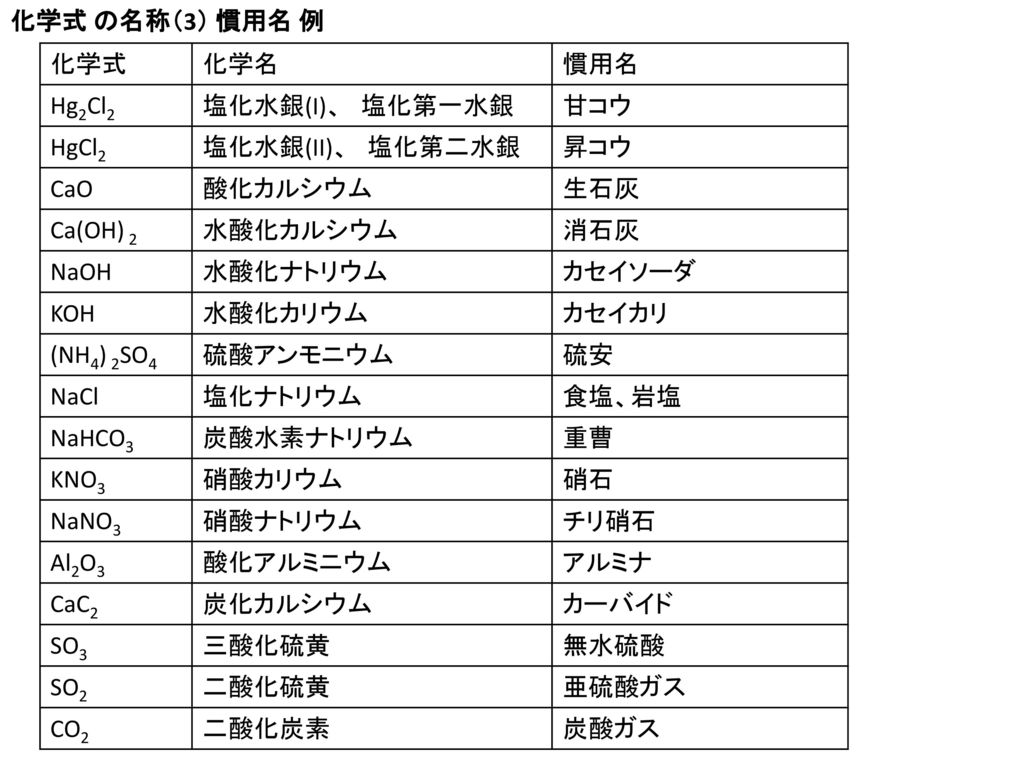
しかし、イオン結晶の中でも、塩化銀 AgCl や硫酸バリウム BaSO 4 などのように、水に難溶なものもあります。そこで、次のような沈殿生成反応が起こります。例えば、 01 mol/L の硝酸銀 AgNO 3 水溶液に、 01 mol/L の希塩酸 HCl を加えると、塩化銀 AgCl の白色沈殿各化学式の係数をa,b,c,dとおくと, a C 2 H 2 +b O 2 →c CO 2 +d H 2 O となりますね。両辺の各原子の数は互いに等しいはずだから,次の関係が成り立つ。 Cの係数から 2a =c Hの係数から 2a =2d Oの係数から 2b =2c +d a を1とすると,c =2,d =1,b =5/2硝酸銀(I)(しょうさんぎん いち英 silver(I) nitrate )は組成式 AgNO 3 、式量 169 の銀の硝酸塩である。 日本の法令では毒物及び劇物取締法により劇物に指定される。 銀を硝酸に溶かすと得られる。
塩素イオンと硝酸銀が反応すると白色沈殿が出来ることを確認する 準備 硝酸銀水溶液、蒸留水、水道水、塩化ナトリウム、試験管3本、試験管立て、薬さじ 実験場所 教室、化学実験室 方法 ① 最初に硝酸銀の説明をします。しかし、イオン結晶の中でも、塩化銀 AgCl や硫酸バリウム BaSO 4 などのように、水に難溶なものもあります。そこで、次のような沈殿生成反応が起こります。例えば、 01 mol/L の硝酸銀 AgNO 3 水溶液に、 01 mol/L の希塩酸 HCl を加えると、塩化銀 AgCl の白色沈殿001 M硝酸銀(AgNO 3)水溶液は市販品(2,000円/500 ml 化学式 溶解度(g/100 ml) リン酸カルシウム(リン酸三カルシウム) Ca 3(PO 4) 実験で学ぶ化学 41 沈殿の生成及び再溶解の反応式(イオン式)を以下の通りである.
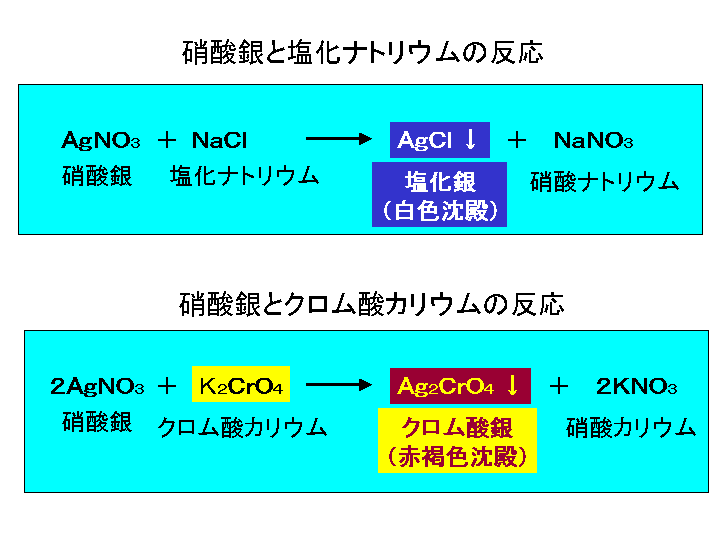
化学 イオン反応式 アエンイオンを含む透明の溶液を試験管に取り,水酸化カリウム水溶液を 少しずつ加えていくと一度白くにごり,加え続けると透明になった。 とあるのですが、これはどのようなイオ 質問No塩化ナトリウムと硝酸銀の反応 塩化ナトリウム + 硝酸銀 → 塩化銀(白色沈殿)+ 硝酸ナトリウム NaCl + AgNO₃ → AgCl + NaNO₃ 以上、『試験・テストに出る化学反応式一覧』を紹介しました。 中学理科で学ぶ化学反応式の一覧を紹介しました。塩化ナトリウムと硝酸銀の反応 塩化ナトリウム + 硝酸銀 → 塩化銀(白色沈殿)+ 硝酸ナトリウム NaCl + AgNO₃ → AgCl + NaNO₃ 以上、『試験・テストに出る化学反応式一覧』を紹介しました。 中学理科で学ぶ化学反応式の一覧を紹介しました。


第4節 遷移金属とその化合物


5 1 化学反応式 おのれー Note
硝酸銀の沈殿反応 硝酸銀はアンモニア水溶液(NH4OH)と反応するものなのでしょうか? 硝酸銀が塩化水素や食塩と反応し、塩化銀の白色沈殿を作るのはわかりました。 ですが、硝酸銀をアンモニア水溶液に加えたところ、赤褐色の繊維質っぽい沈殿(?2sにより白色沈殿。 cl-,so 4 2-により白色沈殿。cro 4 2-により黄色沈殿。oh-により白色 沈殿,さらに過剰のnaohaqにより沈殿が溶解(無色溶液)。 so 4 2-,co 3 2-により白色沈殿。炎色反応で橙色。 so 4 2-,co 3 2-により白色沈殿。炎色反応で黄緑色。硝酸銀の沈殿反応 硝酸銀はアンモニア水溶液(NH4OH)と反応するものなのでしょうか? 硝酸銀が塩化水素や食塩と反応し、塩化銀の白色沈殿を作るのはわかりました。 ですが、硝酸銀をアンモニア水溶液に加えたところ、赤褐色の繊維質っぽい沈殿(?



中学校理科 第1分野 化学変化とイオン Wikibooks



銅 銀イオン定性実験で失敗 なんとなく実験しています
硝酸銀水溶液にアンモニア水を加えると、一時的に少量の水酸化銀 AgOH の白色沈殿ができる。Ag OH – → AgOH ↓ この水酸化銀 AgOH は不安定で、すぐに酸化銀 Ag 2 O の暗褐色沈殿となる。 2Ag 2OH – → Ag 2 O ↓ H 2 O2sにより白色沈殿。 cl-,so 4 2-により白色沈殿。cro 4 2-により黄色沈殿。oh-により白色 沈殿,さらに過剰のnaohaqにより沈殿が溶解(無色溶液)。 so 4 2-,co 3 2-により白色沈殿。炎色反応で橙色。 so 4 2-,co 3 2-により白色沈殿。炎色反応で黄緑色。硝酸銀(I)(しょうさんぎん いち英 silver(I) nitrate )は組成式 AgNO 3 、式量 169 の銀の硝酸塩である。 日本の法令では毒物及び劇物取締法により劇物に指定される。 銀を硝酸に溶かすと得られる。


銀金屬 硝酸銀



臭素酸銀 I Wikipedia
硝酸銀は塩化物イオンと反応して沈殿を生成する。滴定の終点を決定する指示 薬としてウラニン(フルオレセインナトリウム)を用いる。 塩化ナトリウムの溶液に硝酸銀を加えた とき、塩化銀が生成される。 NaCl AgNO3→AgCl NaNO3硝酸銀(agno 3 )液、チオシアン酸アンモニウム(nh 4 scn)液 硝酸銀は、ハロゲン化物イオン、チオシアン酸イオン(scn - )などと1:1で反応し、沈殿を生じる。また、チオシアン酸アンモニウムは、銀イオンと反応し沈殿を生じる。 <標準試薬について>硝酸銀(I)(しょうさんぎん いち英 silver(I) nitrate )は組成式 AgNO 3 、式量 169 の銀の硝酸塩である。 日本の法令では毒物及び劇物取締法により劇物に指定される。 銀を硝酸に溶かすと得られる。


質問箱



14年 平成26年度 日本留考真题化学 知乎
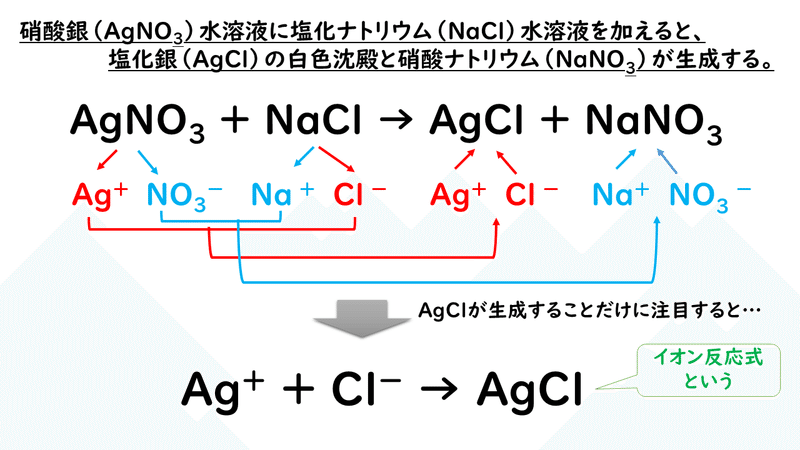
(1) 系統分離 何種類かの陽イオンが含まれている混合物から、各イオンを分離し、イオンを決定することを、「陽イオンの定性分析 (cation analysis) 」といいます。 含まれているイオンが既知で、かつ 2 、 3 種類であるときは、たいてい何通りもの分析方法がありえます。例えば,硝酸銀 AgNO 3 水溶液と塩化ナトリウム水溶液を混合すると,塩化銀 AgCl が沈殿するという反応を考えよう。まず,化学反応式は以下のようになる。 AgNO 3 + NaCl → AgCl↓ + NaNO 3ある水溶液に硝酸銀水溶液を入れると、白色沈殿が生じた、 この時の白色沈殿は、水に溶けにくい塩化銀が生じて起こるものです。 なので、水溶液には塩素が含まれる、というわけです。 わかりましたか?質問あったらどうぞ!



なんで沈殿するのは塩化銀ってわかるんですか 硝酸ナトリウムは違うんですか Clear



化学基礎112c 化学基礎05 13硝酸銀水溶液白色沈殿塩化銀塩素塩化物イオン炎色反応ナトリウム Youtube
B 塩化ナトリウム水溶液に硝酸銀水溶液を加えると,白色の沈殿が生じる。 c 大理石に希塩酸を注いだときに発生する気体を石灰水に通じると,白くにごる。 ① aのみ ② bのみ ③ cのみ ④ aとb ⑤ aとc ⑥ bとc1/121 覚えたい元素記号と化学式 何度も繰り返して覚えよう! 元素記号 は原子番号を示す。 44!これだけ覚えれば,大学入試も完璧です。 1水素 H 2ヘリウム He 3リチウム Li 4ベリリウム Be 5ホウ素 B 6炭素 C 7窒素(チッ素) N 8酸素 O 9フッ素 Fブリタニカ国際大百科事典 小項目事典 硝酸銀の用語解説 化学式 AgNO3 。無色結晶。融点 212℃。有毒。有機物を含むと光によって徐々に黒化する。水,アルコールに可溶。写真乳剤,鏡,銀メッキ液,各種銀塩の製造,毛髪染め,陶磁器の着色,分析用試薬などに用いられるが,古代エジプト


銀滴定法によるしょう油中の食塩の定量 沈殿滴定



Woa1 銀イオン抗菌液の生成方法 その方法で生成される銀イオン抗菌液及びその抗菌液を含有した銀イオン含有製品 Google Patents


化学のイオン反応式についての質問です イオン反応式で表せという Yahoo 知恵袋


3章 イオン結合とイオン結晶 最終回 3 2 イオン結晶の構造 Ppt Download


第61章 実験 銀イオンと鉛イオン



指示薬まとめ 中学理科 ポイントまとめと整理



センター試験にでる化学反応式 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc



銀が溶けた溶液に少量のアンモニア水を加えた時のイオン反応式をかけ 化学 教えて Goo



Woa1 銀イオン抗菌液の生成方法 その方法で生成される銀イオン抗菌液及びその抗菌液を含有した銀イオン含有製品 Google Patents


硝酸銀 I You Iggy
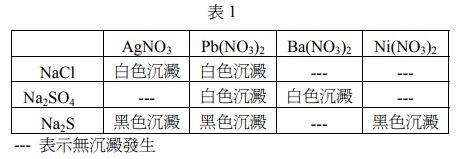


重新載圖6 7為題組 表1是硝酸銀 硝酸鉛 硝酸鋇 硝酸鎳等四種 阿摩線上測驗



食塩水に硝酸銀水溶液を加えた時の反応で 化学反応式は Nacl Agno3 N 化学 教えて Goo
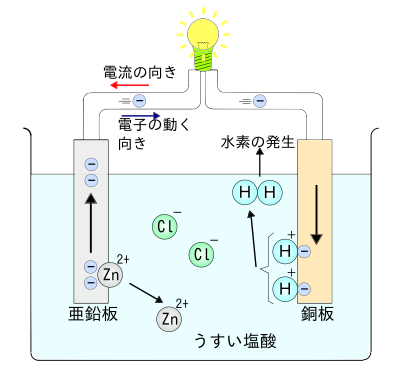


中学校理科 第1分野 化学変化とイオン Wikibooks



これの 2 がわかりません ちなみに答えは塩素でした Clear


第61章 実験 銀イオンと鉛イオン



銅 銀イオン定性実験で失敗 なんとなく実験しています



化成品 硝酸銀 大浦貴金属工業株式会社


Quantity Of Material Ionic Reaction Formula



Woa1 銀イオン抗菌液の生成方法 その方法で生成される銀イオン抗菌液及びその抗菌液を含有した銀イオン含有製品 Google Patents



蛋白質體學 國立陽明大學


硝酸銀水溶液に塩素を通じると生成する物質は何ですか 塩化銀で Yahoo 知恵袋



化学 1 Flashcards Quizlet
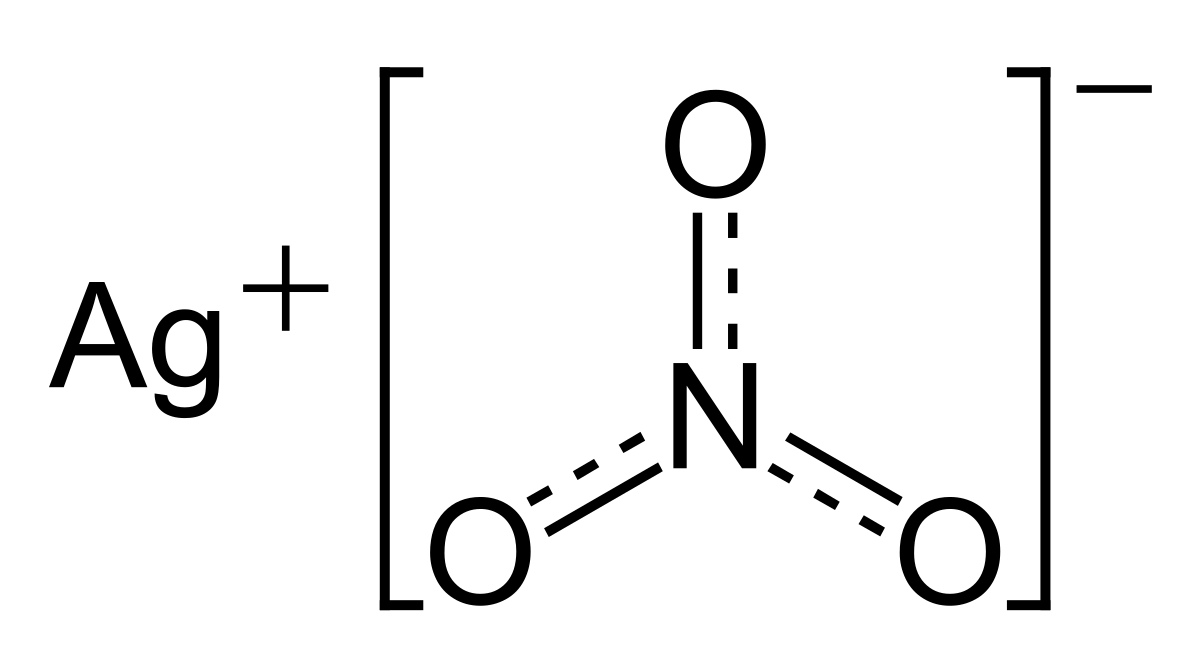


硝酸銀 維基百科 自由的百科全書


铯化金 金的化合物 金化学式 氢氧化金



37の 4 についての質問です 塩化銀の白色沈殿 をどうや 化学に関する質問 勉強質問サイト


何度もすみません 化学基礎です 酸化還元反応を含まないものとしてどう Yahoo 知恵袋


酸化銀 I Iii You Iggy


アセチレンとアンモニア性硝酸銀水溶液の反応式をおしえてくださ Yahoo 知恵袋



Microsoft Word 化学実験 工 先進工 共通 テキスト 第3q Docx Pdf Free Download



アンモニア性硝酸銀水溶液の反応 アルデヒドをアンモニア性硝酸 化学に関する質問 勉強質問サイト



塩化物イオンの定量の硝酸銀水溶液を使用した滴定が良く分かりません 説明お願いします Clear
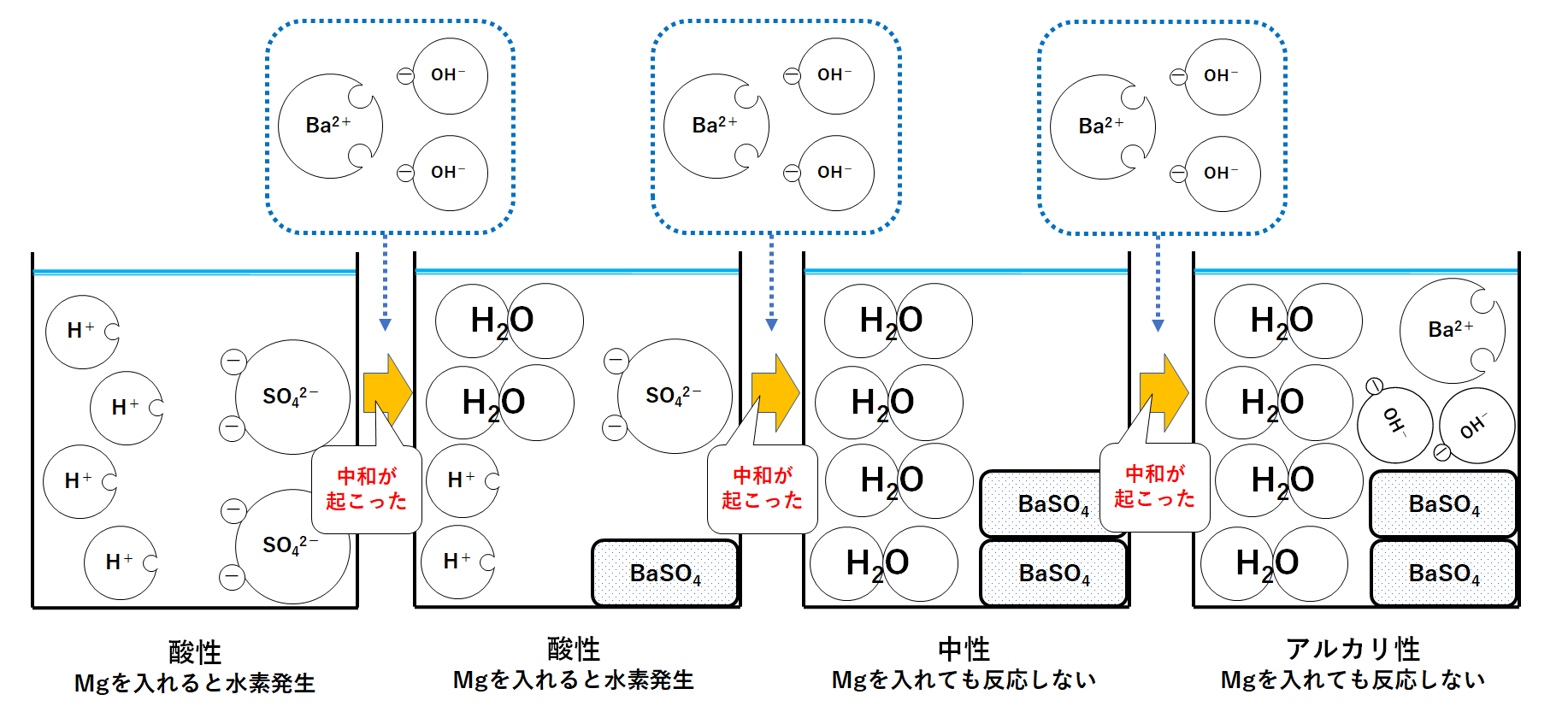


中3化学 沈殿が生じる中和反応 中学理科 ポイントまとめと整理



語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog


銀被膜の形成剤及び形成方法



化学 化学に関する質問 勉強質問サイト



実験化学 43
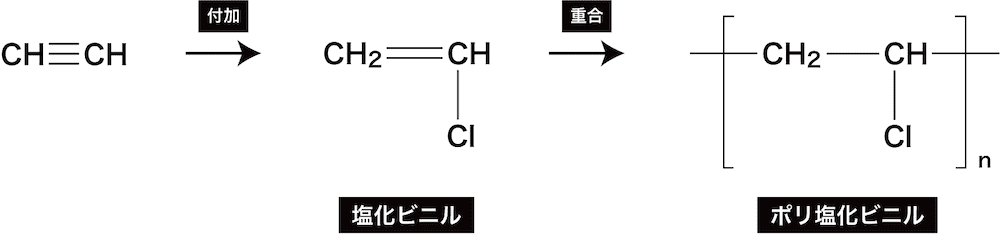


アルキン 一般式の作り方 一覧 製法 付加重合 置換反応など 化学のグルメ



語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog



高校化学 ハロゲン化銀 映像授業のtry It トライイット


2 有關硝酸鋁 硝酸銅 硝酸鋇及硝酸銀之混合液 其分析流程如下 試寫出a 阿摩線上測驗



金属イオンの溶液と沈殿 金属イオンの色の変化の観察 化学授業実践記録 アーカイブ一覧 理科 高等学校 知が啓く 教科書の啓林館



教科書のこの説明の意味がわかりません Clear



高校化学 ハロゲン化銀と沈殿 映像授業のtry It トライイット


第4節 遷移金属とその化合物



金属イオンの溶液と沈殿 金属イオンの色の変化の観察 化学授業実践記録 アーカイブ一覧 理科 高等学校 知が啓く 教科書の啓林館


無機化学 沈殿生成反応



最高のマインクラフト 75 塩化マグネシウム 化学式



メルカリ 藤田保健衛生大学 医学部医学科 参考書 2 100 中古や未使用のフリマ
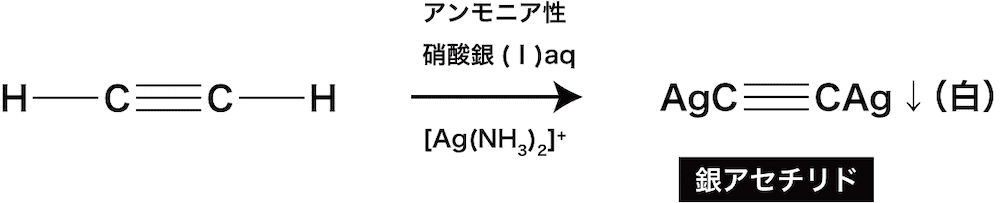


アルキン 一般式の作り方 一覧 製法 付加重合 置換反応など 化学のグルメ



0 件のコメント:
コメントを投稿